Hoá học 9 bài 8: một vài bazơ quan tiền trọng giúp các em học viên lớp 9 nắm rõ kiến thức về phân loại, đặc điểm hóa học với dấu hiệu nhận biết của bazơ. Đồng thời giải cấp tốc được các bài tập hóa học 9 chương 1 trang 27, 30.
Bạn đang xem: Giải bài tập hóa học 9
Việc giải Hóa 9 bài bác 8 trước khi đến lớp các em hối hả nắm vững kỹ năng và kiến thức hôm sau nghỉ ngơi trên lớp sẽ học gì, đọc sơ qua về ngôn từ học. Đồng thời góp thầy cô tham khảo, hối hả soạn giáo án cho học sinh của mình. Vậy sau đây là nội dung cụ thể tài liệu, mời chúng ta cùng xem thêm tại đây.
Giải Hóa 9 bài 8: một trong những bazơ quan lại trọng
Lý thuyết Hóa 9 bài xích 8 một vài bazơ quan tiền trọngGiải bài tập Hóa 9 bài bác 8 trang 27Giải bài xích tập Hóa 9 bài 8 trang 30
Lý thuyết Hóa 9 bài 8 một số trong những bazơ quan lại trọng
A. Natri hiđroxit Na
OH
I. Tính chất vật lí
- Natri hiđroxit là chất rắn không màu, hút ẩm mạnh, tan những trong nước với tỏa nhiệt.
- hỗn hợp Na
OH có tính nhờn, làm cho bục vải vóc giấy và làm mòn da. Khi sử dụng Na
OH phải rất là cẩn thận.
II. đặc điểm hóa học
Natri hiđroxit có không thiếu tính hóa học của một bazơ rã (kiềm).
1. Có tác dụng đổi màu chất chỉ thị.
Dung dịch Na
OH làm chuyển màu sắc qùy tím thành xanh, dung dịch phenolphatalein ko màu thành color đỏ.
2. Chức năng với axit chế tác thành muối với nước (phản ứng trung hòa)
Thí dụ: Na
OH + HCl → Na
Cl + H2O
2Na
OH + H2SO4 → Na2SO4 + H2O
3. Công dụng với axit chế tạo thành muối cùng nước (phản ứng trung hòa)
Thí dụ: 2Na
OH + CO2 → Na2CO3 + H2O
2Na
OH + SO2 → Na2SO3 + H2O
(khi Na
OH công dụng với CO2, SO2 còn hoàn toàn có thể tạo ra muối axit Na
HCO3, NHSO3)
4. Tính năng với dung dịch muối.
Thí dụ: 2 Na
OH + Cu
SO4 → Na2SO4 + Cu(OH)2↓
III. Ứng dụng
Natri hiđroxit có nhiều ứng dụng trong đời sống cùng trong sản xuất. Nó được sử dụng trong:
- chế tạo xà phòng, hóa học tẩy rửa, bột giặt.
- tiếp tế giấy, tơ nhân tạo, trong bào chế dầu mỏ.
- thêm vào nhôm (làm sạch sẽ quặng nhôm trước lúc sản xuất).
IV. Thêm vào Natri hiđroxit
Trong công nghiệp, Na
OH được phân phối bằng phương thức điện phân dung dịch Na
Cl bão hòa. Thùng năng lượng điện phân bao gồm màng chống giữa cực âm và rất dương.
2Na
Cl + 2H2O 2Na
OH + H2 + Cl2
B. Canxi hiđroxit Ca(OH)2
I. Tính chất dung dịch can xi hiđroxit
Để có dung dịch can xi hiđroxit (hay nước vôi trong), ta tổng hợp một ít vôi tôi Ca(OH)2 vào nước được vôi nước (hay vôi sữa). Lọc vôi nước, chất lỏng chiếm được là dung dịch Ca(OH)2.
II. Tính chất hóa học
Dung dịch can xi hiđroxit: Ca(OH)2 tất cả những đặc điểm của một bazơ tan.
1. Làm chuyển màu qùy tím thành xanh, dung dịch phenolphatalein không màu thành color đỏ.
2. Chức năng với axit, chế tác thành muối với nước (phản ứng trung hòa)
Thí dụ: Ca(OH)2 + 2HCl → Ca
Cl2 + 2H2O
Ca(OH)2 + H2SO4 → Ca
SO4 + H2O
3. Tính năng với axit sản xuất thành muối cùng nước (phản ứng trung hòa)
Thí dụ: Ca(OH)2 + CO2 → Ca
CO3↓ + H2O
Ca(OH)2 + SO2 → Ca2SO3 + H2O
4. Công dụng với dung dịch muối.
Thí dụ: Ca(OH)2 + Na2CO3 → Ca
CO3↓ + 2Na
OH
III. Ứng dụng
Canxi hiđroxit được dùng:
- Làm vật tư trong xây dựng.
- Khử chua đất trồng trọt.
-Khử độc các chất thải công nghiệp, khử trùng chất thải sinh hoạt và xác bị tiêu diệt động vật…
Giải bài xích tập Hóa 9 bài bác 8 trang 27
Câu 1
Có 3 lọ không nhãn, mỗi lọ đựng một chất rắn sau: Na
OH, Ba(OH)2, Na
Cl. Hãy trình diễn cách phân biệt chất đựng trong những lọ bằng phương thức hóa học. Viết những phương trình hóa học giả dụ có.
Gợi ý đáp án
Lấy chủng loại thử từng hóa học và đặt số thứ tự. Hòa tan những mẫu thử vào H2O rồi thử những dung dịch:
- cần sử dụng quỳ tím bỏ vô từng chủng loại thử
+ chủng loại nào làm cho quỳ tím hóa xanh đó là Na
OH và Ba(OH)2.
+ còn lại là Na
Cl không có hiện tượng.
- mang đến H2SO4 vào các mẫu thử Na
OH và Ba(OH)2
+ mẫu nào gồm kết tủa trắng đó là thành phầm của Ba(OH)2
PTHH: Ba(OH)2 + H2SO4 → Ba
SO4↓ white + 2H2O
+ còn sót lại là Na
OH.
Câu 2
Có hồ hết chất sau: Zn, Zn(OH)2, Na
OH, Fe(OH)3, Cu
SO4, Na
Cl, HCl. Hãy chọn những chất thích hợp điền vào sơ thiết bị phản ứng sau với lập phương trình hóa học.
a) ... → Fe2O3 + H2O
b) H2SO4 + ... → Na2SO4 + H2
c) H2SO4 + ... → Zn
SO4 + H2O
d) Na
OH + ... → Na
Cl + H2O
e) ... + CO2 → Na2CO3 + H2O.
Gợi ý đáp án
a) 2Fe(OH)3 → Fe2O3 + 3H2O
b) H2SO4 + 2Na
OH → Na2SO4 + 2H2O
c) H2SO4 + Zn(OH)2 → Zn
SO4 + 2H2O
d) Na
OH + HCl → Na
Cl + H2O
e) 2Na
OH + CO2 → Na2CO3 + H2O.
Câu 3
Dẫn nhàn hạ 1,568 lít khí CO2(đktc) vào trong 1 dung dịch tất cả hòa tung 6,4g Na
OH.
a) chất nào đã lấy dư cùng dư là từng nào (lít hoặc gam)?
b) Hãy xác minh muối chiếm được sau bội phản ứng.
Gợi ý đáp án
n
CO2 =1,568/22,4 = 0,07 mol; n
NaOH =6,4/40 = 0,16 mol
2Na
OH + CO2 → Na2CO3 + H2O
Bđ: 0,16 0,07 (mol)
Pứ: 0,14 0,07 → 0,07 0,07
Spứ: 0,02 0 0,07
a) Theo phương trình phản ứng Na
OH dư, CO2 bội phản ứng hết, khối lượng Na
OH dư: 0,02 × 40 = 0,8 g
b) trọng lượng muối Na2CO3 tạo ra thành là: 0,07 × 106 = 7,42 g.
Giải bài xích tập Hóa 9 bài xích 8 trang 30
Câu 1
Viết các phương trình hóa học tiến hành các biến hóa hóa học sau:
Gợi ý đáp án
Phương trình hóa học của những phản ứng:
(1) Ca
CO3

O + CO2
(2) Ca
O + H2O → Ca(OH)2
(3) Ca(OH)2 + CO2 → Ca
CO3 + H2O
(4) Ca
O + 2HCl → Ca
Cl2 + H2O
(5) Ca(OH)2 + 2HNO3 → Ca(NO3)2 + 2H2O
Câu 2
Có ba lọ ko nhãn, mỗi lọ đựng 1 trong các ba hóa học rắn white color sau: Ca
CO3, Ca(OH)2, Ca
O. Hãy nhận thấy chất đựng trong mỗi lọ bằng phương thức hóa học. Viết phương trình hóa học.
Gợi ý đáp án
Lấy mỗi chất rắn 1 ít làm mẫu thử cùng đánh số sản phẩm công nghệ tự
- Cho bố chất rắn vào nước:
+ chất nào ko tan trong nước chính là Ca
CO3.
+ chất nào phản ứng cùng với nước có tác dụng nóng ống nghiệm là Ca
O
PTHH: Ca
O + H2O → Ca(OH)2
+ hóa học chỉ tan 1 phần tạo hóa học lỏng màu trắng và có một trong những phần kết tủa lắng dưới đáy là Ca(OH)2
Câu 3
Hãy viết những phương trình chất hóa học khi mang đến dung dịch Na
OH công dụng với hỗn hợp H2SO4 tạo ra ra:
a) muối hạt natri hiđrosunfat.
b) muối bột natri sunfat.
Gợi ý đáp án
a) muối hạt natri hidrosunfat: Na
HSO4
H2SO4 + Na
OH → Na
HSO4 + H2O
b) muối natri sunfat: Na2SO4
H2SO4 + 2Na
OH → Na2SO4 + 2H2O
Câu 4
Một dung dịch bão trung khí CO2 vào nước gồm p
H = 4. Hãy lý giải và viết phương trình hóa học của CO2 cùng với nước.
Gợi ý đáp án
Dung dịch bão hòa CO2 vào nước tạo ra dung dịch axit cacbonic (H2CO3) là axit yếu, gồm p
H = 4.
Giải vở bài xích tập chất hóa học 9 bài bác 8: một trong những bazơ quan trọng: canxi Hidroxit ( Ca(OH)2 )

Nhằm mục tiêu giúp học tập sinh thuận lợi làm bài tập về công ty trong Vở bài tập chất hóa học lớp 9, công ty chúng tôi biên biên soạn giải vở bài xích tập chất hóa học lớp 9 bài bác 8: một số bazơ quan liêu trọng: can xi Hidroxit ( Ca(OH)2 ) tuyệt nhất, ngắn gọn bám đít nội dung giấy tờ bài tập chất hóa học 9.
Học theo Sách giáo khoa
I. TÍNH CHẤT CỦA Ca(OH)2
1. Ca(OH)2 có đặc thù hóa học của một bazơ tan.
a) Làm chuyển màu qùy tím thành xanh, hỗn hợp phenolphatalein ko màu thành màu hồng.
b) Ca(OH)2 tính năng với axit, thành phầm là muối cùng nước (phản ứng trung hòa)
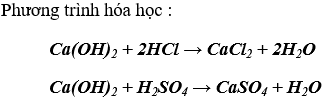
c) hỗn hợp Ca(OH)2 chức năng với oxit axit sản phẩm là muối với nước
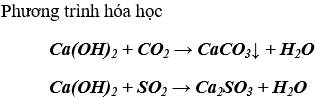
2. Ứng dụng
- Làm vật tư trong xây dựng.
- Khử chua đất trồng trọt.
- Khử độc những chất thải công nghiệp, khử trùng chất thải sinh hoạt với xác chết động vật…
II. THANG p
H
PH = 7: dung dịch là trung tính ví dụ : nước cất có PH = 7
PH axit, PH càng nhỏ dại độ axit càng lớn.
PH > 7: Dung dịch tất cả tính bazơ, PH càng bự độ bazo càng lớn.
Bài tập
Bài 1. (Trang 28 Vở bài xích Tập chất hóa học 9 ) Viết những phương trình hóa học tiến hành những biến hóa hóa học sau:
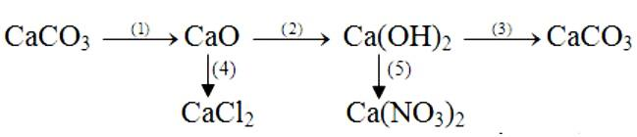
Lời giải:
Các phương trình hóa học
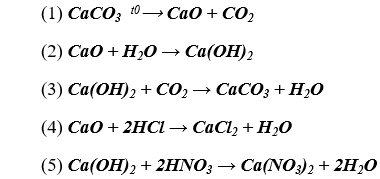
Bài 2. (Trang 28 Vở bài bác Tập chất hóa học 9 ) Có tía lọ ko nhãn, từng lọ đựng một trong ba hóa học rắn màu trắng sau: Ca
CO3, Ca
O, Ca(OH)2 . Hãy nhận thấy chất đựng trong những lọ bằng phương thức hóa học. Viết các phương thức hóa học.
Lời giải:
Nhận biết những chất rắn white color là Ca
CO3 ,Ca
O , Ca(OH)2:
Hòa rã 3 chất rắn bên trên vào nước:
+ chất rắn không tan là Ca
CO3
+ hóa học rắn tan mặt khác tỏa những nhiệt là Ca
O
+ hóa học rắn tan không kèm theo hiện tượng lạ gì là : Ca(OH)2
Các phương trình hóa học: Ca
O + H2O → Ca(OH)2
Bài 3. (Trang 28 Vở bài xích Tập hóa học 9 ) Hãy viết các phương trình chất hóa học của bội nghịch ứng khi mang lại dung dịch Na
OH tác dụng với dung dịch H2SO4 tạo ra:
a) muối bột natri hiđrosunfat.
b) muối natrisunfat.
Lời giải:
Phương trình hóa học của phản bội ứng giữa Na
OH và H2SO4 tạo thành ra:
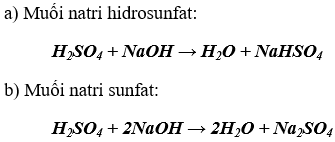
Bài 4. (Trang 28 Vở bài Tập chất hóa học 9 ) Một dung dịch bão trung khí CO2 trong nước có p
H = 4. Hãy giải thích và viết phương trình hóa học của CO2 cùng với nước.
Lời giải:
Giải thích: Dung dịch bão hòa CO2 có p
H = 4, nghĩa là dung dịch tất cả tính axit yếu. Do khí CO2 chức năng với nước chế tạo ra thành axit cacbonic, là một axit khôn cùng yếu
Phương trình hóa học: CO2 + H2O → H2CO3
Bài tập ngã sung
Bài 1. (Trang 29 Vở bài Tập hóa học 9 ) dung dịch HCl khác với dung dịch Na
OH là:
A. Thay đổi màu sắc quì tím
B. Tất cả độ p
H nhỏ tuổi hơn
C. Tính năng với hỗn hợp muối
D. Có phản ứng trung hòa
Lời giải:
Kết quả đúng: A
Dung dịch HCl làm quỳ tím gửi đỏ, hỗn hợp Na
OH làm quỳ tím đưa xanh
Bài 2. (Trang 29 Vở bài bác Tập hóa học 9 ) hỗn hợp nào gồm độ axit mạnh dạn nhất trong các dung dịch là:
A. P
H = 4
B. P
H = 2
C. P
H = 10
D. P
H = 14
Lời giải:
Kết quả đúng: B
p
H = 7: hỗn hợp là trung tính thí dụ : nước cất có p
H = 7
p
H 7: Dung dịch tất cả tính bazơ, p
H càng lớn độ bazo càng lớn.
Bài 3. (Trang 29 Vở bài xích Tập hóa học 9 ) hỗn hợp nào bao gồm độ bazo táo tợn nhất trong các dung dịch là:













